При входе на сайт вы даете согласие на обработку персональных данных в соответствии с пользовательским соглашением
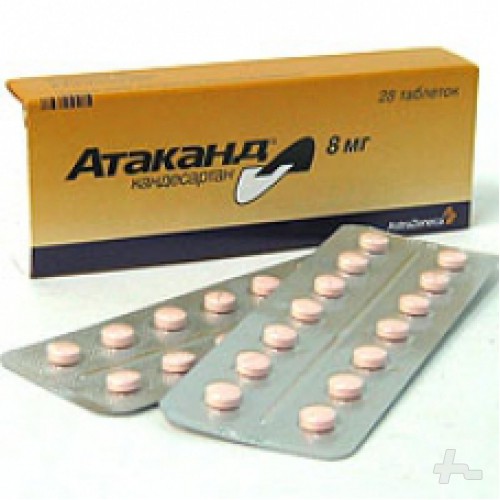
Внешний вид упаковки может отличаться от фотографии





























Атаканд® |
АстраЗенека Фармасьютикалз ООО (Россия)
таблетки 8 мг; блистер 14, пачка картонная 2; код EAN: 7321838741372; № П N014373/01, 2009-03-25 от AstraZeneca AB (Швеция)
Латинское название
Действующее вещество
АТХ:
Фармакологическая группа
Нозологическая классификация (МКБ-10)
I15 Вторичная гипертензия
I50.0 Застойная сердечная недостаточность
I50.1 Левожелудочковая недостаточность
Состав
| Таблетки | 1 табл. |
| активное вещество: | |
| кандесартана цилексетил | 8 мг |
| 16 мг | |
| вспомогательные вещества: кармеллоза кальция (кармеллозы кальциевая соль) — 5,6/5,6 мг; гипролоза (гидроксипропилцеллюлоза) — 4/4 мг; краситель железа оксид красный (E172) — 0,065/0,26 мг; лактозы моногидрат — 89,4/81,4 мг; магния стеарат — 0,4/0,4 мг; кукурузный крахмал — 20/20 мг; макрогол — 2,6/2,6 мг |
Описание лекарственной формы
Атаканд® 8 мг: светло-розовые круглые двояковыпуклые таблетки, с риской и гравировкой «A/CG» — на одной стороне и 008 — на другой.
Атаканд® 16 мг: розовые круглые двояковыпуклые таблетки, с риской и гравировкой «A/CH» — на одной стороне и 016 — на другой.
Фармакологическое действие
Фармакодинамика
Ангиотензин II — основной гормон РААС, который играет важную роль в патогенезе артериальной гипертензии, сердечной недостаточности и других сердечно-сосудистых заболеваний. Основными физиологическими эффектами ангиотензина II являются вазоконстрикция, стимуляция продукции альдостерона, регуляция водно-электролитного гомеостаза и стимуляция клеточного роста. Все эти эффекты опосредованы взаимодействием ангиотензина II с ангиотензиновыми рецепторами 1 типа (АТ1-рецепторы).
Кандесартан — селективный антагонист рецепторов ангиотензина II 1 типа. Кандесартан не ингибирует АПФ, который осуществляет превращение ангиотензина I в ангиотензин II и разрушает брадикинин; не влияет на АПФ и не приводит к накоплению брадикинина или субстанции Р. При сравнении кандесартана с ингибиторами АПФ развитие кашля реже встречалось у пациентов, получавших кандесартана цилексетил. Кандесартан не связывается с рецепторами других гормонов и не блокирует ионные каналы, участвующие в регуляции функций ССС. В результате блокирования АТ1-рецепторов ангиотензина II происходит дозозависимое повышение уровня ренина, ангиотензина I, ангиотензина II и снижение концентрации альдостерона в плазме крови.
Артериальная гипертензия
При артериальной гипертензии кандесартан вызывает дозозависимое длительное снижение АД. Антигипертензивный эффект препарата обусловлен снижением ОПСС, без изменения ЧСС. Не отмечалось случаев выраженной артериальной гипотензии после приема первой дозы препарата, а также синдрома отмены (синдром «рикошета») после прекращения терапии.
Начало гипотензивного действия после приема первой дозы кандесартана цилексетила обычно развивается в течение 2 ч. На фоне продолжающейся терапии препаратом в фиксированной дозе максимальное снижение АД обычно достигается в течение 4 нед и сохраняется на протяжении лечения. Кандесартана цилексетил, назначаемый 1 раз в сутки, обеспечивает эффективное и плавное снижение АД в течение 24 ч с незначительными колебаниями АД в интервалах между приемами очередной дозы препарата. Применение кандесартана цилексетила совместно с гидрохлоротиазидом приводит к усилению гипотензивного эффекта. Совместное применение кандесартана цилексетила и гидрохлоротиазида (или амлодипина) хорошо переносится.
Эффективность препарата не зависит от возраста и пола пациентов.
Кандесартана цилексетил увеличивает почечный кровоток и не изменяет или же повышает скорость клубочковой фильтрации, тогда как почечное сосудистое сопротивление и фильтрационная фракция снижаются. Прием кандесартана цилексетила в дозе 8–16 мг в течение 12 нед не оказывает негативного влияния на уровень глюкозы и липидный профиль у пациентов с артериальной гипертензией и сахарным диабетом типа 2.
Клиническое действие кандесартана цилексетила на уровень заболеваемости и смертности при приеме в дозе 8–16 мг (средняя доза 12 мг) 1 раз в сутки исследовалось в ходе рандомизированного клинического исследования с участием 4937 пожилых пациентов (возраст от 70 до 89 лет, 21% пациентов в возрасте 80 лет и старше) с артериальной гипертензией мягкой и умеренной степени тяжести, получающих терапию кандесартана цилексетилом в среднем в течение 3,7 лет (исследование COPE — исследование когнитивных функций и прогноза у пожилых пациентов). Пациенты получали кандесартан или плацебо, при необходимости, в комбинации с другими антигипертензивными средствами. В группе пациентов, получавших кандесартан, отмечено снижение АД со 166/90 до 145/80 мм рт. ст. и в контрольной группе — со 167/90 до 149/82 мм рт. ст. Статистически значимых различий частоты сердечно-сосудистых осложнений (летальность в результате сердечно-сосудистых заболеваний, частота инфаркта миокарда и инсульта, не приведших к смертельному исходу) между двумя группами пациентов отмечено не было.
В группе пациентов, получавших кандесартан, было отмечено 26,7 случаев возникновения сердечно-сосудистых осложнений на 1000 пациенто-лет по сравнению с 30 случаями на 1000 пациенто-лет в контрольной группе (cоотношение рисков =0,89; 95% доверительный интервал 0,75–1,06; р=0,19).
Хроническая сердечная недостаточность
Согласно результатам исследования CHARM (Кандесартан при хронической сердечной недостаточности — Оценка Снижения Уровня Смертности и Заболеваемости) применение кандесартана цилексетила приводило к снижению частоты летальных исходов и необходимости в госпитализации по поводу хронической сердечной недостаточности и улучшению систолической функции левого желудочка.
Пациенты с хронической сердечной недостаточностью в дополнение к основной терапии получали кандесартана цилексетил в дозе 4–8 мг/сут с повышением дозы до 32 мг/сут или до максимальной переносимой терапевтической дозы (средняя доза кандесартана составляла 24 мг). Медиана длительности наблюдения составляла 37,7 мес. Через 6 мес терапии 63% пациентов, продолжавших принимать кандесартана цилексетил (89%), получали терапевтическую дозу 32 мг.
В другом исследовании CHARM-Alternative (n=2028) участвовали пациенты со сниженной (≤40%) фракцией выброса левого желудочка (ФВЛЖ), не получавшие ингибитор АПФ из-за непереносимости (в основном из-за кашля — 72%); показатели частоты летальных исходов от сердечно-сосудистых заболеваний и первой госпитализации по поводу хронической сердечной недостаточности были значительно ниже в группе пациентов, получавших кандесартан по сравнению с группой плацебо (cоотношение рисков =0,77; 95% доверительный интервал 0,67–0,89; р<0,001). Снижение относительного риска составляло 23%. В этом исследовании для предотвращения одного случая летального исхода от сердечно-сосудистых осложнений или госпитализации по поводу хронической сердечной недостаточности было необходимо проводить лечение 14 пациентов на протяжении всего периода исследования. Комбинированный критерий, включавший в себя частоту летальных исходов вне зависимости от их причин и показатель первой госпитализации по поводу хронической сердечной недостаточности, также оказался значительно ниже в группе пациентов, получавших кандесартан (cоотношение рисков =0,80; 95% доверительный интервал 0,7–0,92; р=0,001). При этом было отмечено положительное влияние кандесартана на каждую из составляющих этого комбинированного критерия — частоту летальных исходов и заболеваемость (показатель частоты госпитализаций по поводу хронической сердечной недостаточности). Применение кандесартана цилексетила приводило к улучшению функционального класса хронической сердечной недостаточности по классификации NYHA (р=0,008).
В исследовании CHARM-Added (n=2548) у пациентов со сниженной ФВЛЖ ≤40%, получавших ингибиторы АПФ, комбинированный критерий, включавший в себя показатель летальности от сердечно-сосудистых заболеваний и первой госпитализации по поводу хронической сердечной недостаточности был значительно ниже в группе пациентов, получавших кандесартан, по сравнению с группой плацебо (cоотношение рисков =0,85; 95% доверительный интервал 0,75–0,96; р=0,011), что соответствовало снижению относительного риска на 15%. В этом исследовании для предотвращения одного случая летального исхода от сердечно-сосудистых осложнений или госпитализации по поводу хронической сердечной недостаточности было необходимо проводить лечение 23 пациентов на протяжении всего периода исследования. Значение комбинированного критерия эффективности, включавшего в себя оценку частоты летальных исходов вне зависимости от их причин или частоты первой госпитализации по поводу хронической сердечной недостаточности, был значительно ниже в группе пациентов, получавших кандесартан (cоотношение рисков =0,87; 95% доверительный интервал 0,78–0,98; р=0,021), что также свидетельствовало о положительном эффекте при применении кандесартана. Применение кандесартана цилексетила приводило к улучшению функционального класса хронической сердечной недостаточности по классификации NYHA (р=0,02).
В исследовании CHARM-Preserve (n=3023) у пациентов с сохраненной систолической функцией (ФВЛЖ >40%) не было выявлено статистически достоверных различий значения комбинированного критерия эффективности, который включал в себя частоту летальных исходов и частоту первой госпитализации по поводу хронической сердечной недостаточности, в группах кандесартана и плацебо (cоотношение рисков =0,89; 95% доверительный интервал 0,77–1,03; р=0,118). Небольшое численное снижение этого критерия было обусловлено снижением частоты госпитализаций по поводу хронической сердечной недостаточности. В данном исследовании не было показано влияния кандесартана на частоту летальных исходов.
При раздельном анализе результатов 3-х исследований программы CHARM не было получено достоверных различий частоты летальных исходов в группах кандесартана и плацебо. Однако частота летальных исходов была оценена в объединенной популяции исследований CHARM-Alternative и CHARM-Added и во всех 3-х исследованиях (cоотношение рисков =0,91; 95% доверительный интервал 0,83–1,0; р=0,055). Снижение частоты летальных исходов и частоты госпитализаций по поводу хронической сердечной недостаточности на фоне терапии кандесартаном не зависело от возраста, пола и сопутствующей терапии. Кандесартан также был эффективен у пациентов, принимавших бета-адреноблокаторы в сочетании с ингибиторами АПФ, при этом эффективность кандесартана не зависела от того, принимает ли пациент оптимальную дозу ингибитора АПФ или нет.
У пациентов с хронической сердечной недостаточностью и сниженной систолической функцией левого желудочка (ФВЛЖ ≤40%), прием кандесартана способствовал снижению ОПСС и капиллярного давления в легких, повышению активности ренина и концентрации ангиотензина II в плазме крови, а также снижению уровня альдостерона.
Фармакокинетика
Всасывание и распределение
Кандесартана цилексетил является пролекарством для приема внутрь. Быстро превращается в активное вещество — кандесартан посредством эфирного гидролиза при всасывании из пищеварительного тракта, прочно связывается с АТ1-рецепторами и медленно диссоциирует, не имеет свойств агониста. Абсолютная биодоступность кандесартана после приема внутрь раствора кандесартана цилексетила составляет около 40%. Относительная биодоступность таблетированного препарата по сравнению с раствором для приема внутрь составляет приблизительно 34%. Таким образом, расчетная абсолютная биодоступность таблетированной формы препарата составляет 14%. Cmax в сыворотке крови достигается через 3–4 ч после приема таблетированной формы препарата. При увеличении дозы препарата в пределах рекомендуемых концентрация кандесартана повышается линейно. Фармакокинетические параметры кандесартана не зависят от пола пациента. Прием пищи не оказывает значимого влияния на AUC, т.е. одновременный прием пищи существенно не влияет на биодоступность препарата. Кандесартан активно связывается с белками плазмы крови (>99%). Vd кандесартана составляет 0,1 л/кг.
Метаболизм и выведение из организма
Кандесартан, в основном, выводится из организма почками и желчью в неизмененном виде и лишь в незначительной степени метаболизируется в печени. T1/2 кандесартана составляет приблизительно 9 ч. Кумуляция в организме не наблюдается.
Общий клиренс кандесартана составляет около 0,37 мл/мин/кг, при этом почечный клиренс — около 0,19 мл/мин/кг. Почечная экскреция кандесартана осуществляется путем клубочковой фильтрации и активной канальцевой секреции. При приеме внутрь радиоактивно-меченного кандесартана цилексетила около 26% от введенного количества выводится почками в виде кандесартана и 7% — в виде неактивного метаболита, тогда как в кале обнаруживается 56% от введенного количества в виде кандесартана и 10% — в виде неактивного метаболита.
У пожилых больных (старше 65 лет) Cmax и AUC кандесартана увеличиваются на 50 и 80% соответственно, по сравнению с молодыми пациентами. Однако, гипотензивный эффект и частота возникновения побочных эффектов при применении Атаканда® не зависят от возраста пациентов.
У пациентов с легким и умеренным нарушением функции почек Cmax и AUC кандесартана увеличивались на 50 и 70% соответственно, тогда как T1/2 препарата не изменялся по сравнению с больными с нормальной функцией почек. У пациентов с тяжелым нарушением функции почек Cmax и AUC кандесартана увеличивались на 50 и 110% соответственно, а T1/2 препарата увеличивался в 2 раза. У пациентов, находящихся на гемодиализе, были выявлены такие же фармакокинетические параметры кандесартана, как у пациентов с тяжелым нарушением функции почек.
У пациентов с легким и умеренным нарушением функции печени отмечалось повышение AUC кандесартана на 23%.
Показания препарата Атаканд®
артериальная гипертензия;
хроническая сердечная недостаточность и нарушение систолической функции левого желудочка (снижение фракции выброса левого желудочка ≤40%) в качестве дополнительной терапии к ингибиторам АПФ или при непереносимости ингибиторов АПФ (см. раздел «Фармакодинамика»).
Противопоказания
повышенная чувствительность к кандесартана цилексетилу или другим компонентам, входящим в состав препарата;
выраженные нарушения функции печени и/или холестаз;
беременность и период лактации (см. раздел «Применение при беременности и кормлении грудью»).
С осторожностью: у больных с выраженной почечной недостаточностью (Cl креатинина <30 мл/мин), двухсторонним стенозом почечных артерий или стенозом артерии единственной почки, с гемодинамически значимым стенозом аортального и митрального клапана, после пересадки почки в анамнезе, у больных с цереброваскулярными заболеваниями и ИБС, гиперкалиемией, у больных со сниженным ОЦК, первичным гиперальдостеронизмом (отсутствует достаточное количество данных по клиническим исследованиям), гипертрофической кардиомиопатией, в возрасте до 18 лет (эффективность и безопасность не установлены).
Применение при беременности и кормлении грудью
У человеческого эмбриона система кровоснабжения почки, которая зависит от развития РААС, начинает формироваться во II триместре беременности. Таким образом, риск для плода увеличивается при назначении Атаканда® во II и III триместрах беременности. Препараты, оказывающие прямое действие на РААС, могут вызывать нарушения развития плода или оказывать негативное действие на новорожденного вплоть до летального исхода при применении препарата во II и III триместрах беременности.
В исследованиях на животных выявлено повреждение почек в эмбриональном и неонатальном периодах при применении кандесартана цилексетила. Предполагается, что механизм повреждения обусловлен фармакологическим воздействием препарата на РААС.
Основываясь на полученной информации, не следует применять Атаканд® во время беременности. Если беременность выявлена в период лечения Атакандом®, терапия должна быть прекращена (см. раздел «Противопоказания»).
В настоящее время неизвестно, проникает ли кандесартан в грудное молоко. В связи с возможным нежелательным действием на грудных детей, Атаканд® не следует применять в период грудного кормления.
Побочные действия
Артериальная гипертензия
Побочные эффекты в ходе клинических исследований носили умеренный и преходящий характер и были сопоставимы по частоте с группой плацебо. Общая частота возникновения побочных эффектов на фоне приема Атаканда® не зависела от дозы препарата и возраста пациента. Частота случаев прекращения терапии в связи с побочными эффектами была сходной при использовании кандесартана цилексетила (2,4%) и плацебо (2,6%).
В ходе анализа данных проведенных исследований сообщалось о следующих побочных эффектах, часто (>1/100) встречавшихся на фоне приема кандесартана цилексетила. Описанные побочные эффекты наблюдались с частотой хотя бы на 1% больше, чем в группе плацебо.
Со стороны ЦНС: головокружение, слабость, головная боль.
Со стороны костно-мышечной системы, соединительной ткани: боль в спине.
Инфекции: респираторные инфекции.
Лабораторные показатели: в целом при применении Атаканда® не было отмечено клинически значимых изменений стандартных лабораторных показателей. Как и при применении других ингибиторов РААС, может наблюдаться небольшое снижение концентрации гемоглобина. Наблюдалось увеличение содержания креатинина, мочевины или калия и уменьшение содержания натрия. Повышение уровня АЛТ было отмечено несколько чаще при применении Атаканда® в сравнении с плацебо (1,3% вместо 0,5%). При применении Атаканда® обычно не требуется регулярного контроля лабораторных показателей. Однако у пациентов с нарушением функции почек рекомендуется периодически контролировать уровень калия и креатинина в сыворотке крови.
Хроническая сердечная недостаточность
Побочные эффекты, выявленные на фоне применения Атаканда® у пациентов с хронической сердечной недостаточностью, соответствовали фармакологическим свойствам препарата и зависели от состояния пациента. В ходе клинических исследований CHARM проводилось сравнение Атаканда® в дозах до 32 мг (n = 3803) с плацебо (n = 3796), 21% пациентов из группы пациентов, получавших кандесартана цилексетил, и 16,1% пациентов из группы пациентов, получавших плацебо, прекратили лечение из-за возникновения побочных реакций.
Наиболее часто встречающиеся побочные эффекты (≥1/100, <1/10).
Со стороны ССС: выраженное снижение АД.
Со стороны мочевыводящей системы: нарушение функции почек.
Лабораторные изменения: повышение уровня креатинина, мочевины и калия. Рекомендуется контролировать уровень креатинина и калия в сыворотке крови.
О следующих побочных эффектах в ходе постмаркетингового применения препарата докладывалось очень редко (<1/10000).
Со стороны кровеносной и лимфатической системы: лейкопения, нейтропения и агранулоцитоз.
Нарушение метаболизма и заболевания, вызванные нарушением метаболизма: гиперкалиемия, гипонатриемия.
Со стороны нервной системы: головокружение, слабость, головная боль.
Со стороны ЖКТ: тошнота.
Со стороны печени и желчевыводящих путей: повышение активности печеночных ферментов, нарушение функции печени или гепатит.
Аллергические реакции: ангионевротический отек, кожная сыпь, крапивница, кожный зуд.
Со стороны костно-мышечной системы, соединительной ткани: боль в спине, артралгия, миалгия.
Со стороны мочевыводящей системы: нарушение функции почек, включая почечную недостаточность у предрасположенных пациентов.
Взаимодействие
В фармакокинетических исследованиях было изучено сочетанное применение Атаканда® с гидрохлоротиазидом, варфарином, дигоксином, пероральными контрацептивами (этинилэстрадиол/левоноргестрел), глибенкламидом, нифедипином и эналаприлом. Клинически значимых лекарственных взаимодействий выявлено не было.
Кандесартан метаболизируется в печени в незначительной степени (CYP2C9). Проведенные исследования по взаимодействию не выявили влияния препарата на CYP2C9 и CYP3A4; действие на другие изоферменты системы цитохрома Р450 не изучено.
Совместное применение Атаканда® с другими антигипертензивными средствами потенцирует гипотензивный эффект.
Опыт применения других ЛС, действующих на РААС, показывает, что сопутствующая терапия калийсберегающими диуретиками, препаратами калия, заменителями соли, содержащими калий, и другими средствами, которые могут повышать уровень калия в сыворотке крови (например, гепарин) может приводить к развитию гиперкалиемии.
При сочетанном назначении препаратов лития с ингибиторами АПФ сообщалось об обратимом повышении концентрации лития в сыворотке крови и развитии токсических реакций. Подобные реакции могут встречаться и при применении антагонистов рецепторов ангиотензина II, в связи с чем, рекомендуется контролировать уровень лития в сыворотке крови при комбинированном применении этих препаратов.
Биодоступность кандесартана не зависит от приема пищи.
Способ применения и дозы
Внутрь, 1 раз в сутки вне зависимости от приема пищи.
Артериальная гипертензия
Рекомендуемая начальная и поддерживающая доза Атаканда® составляет 8 мг 1 раз в сутки. Пациентам, которым требуется дальнейшее снижение АД, рекомендуется увеличить дозу до 16 мг 1 раз в сутки. Максимальный антигипертензивный эффект достигается в течение 4 нед от начала лечения.
В случае, если терапия Атакандом® не приводит к снижению АД до оптимального уровня, рекомендуется добавить к терапии тиазидный диуретик.
Пациенты пожилого возраста. У пациентов пожилого возраста нет необходимости корректировать начальную дозу препарата.
Пациенты с нарушением функции почек. У пациентов с легким или умеренным нарушением функции почек (Cl креатинина ≥30 мл/мин/1,73м2 площади поверхности тела) не требуется изменение начальной дозы препарата.
Клинический опыт применения препарата у пациентов с тяжелым нарушением функции почек (Cl креатинина <30 мл/мин/1,73 м2 площади поверхности тела) ограничен; в этом случае следует рассмотреть возможность начала лечения с суточной дозы 4 мг.
Пациенты с нарушением функции печени. У пациентов с нарушением функции печени легкой и средней степени тяжести рекомендуется начинать лечение с суточной дозы 2 мг 1 раз в сутки. Возможно увеличение дозы при необходимости. Клинический опыт применения у больных с тяжелыми поражениями печени ограничен.
Сопутствующая терапия. Применение Атаканда® совместно с диуретиками тиазидного типа (например гидрохлоротиазид) могут усилить гипотензивный эффект Атаканда®.
Хроническая сердечная недостаточность
Рекомендуемая начальная доза Атаканда® составляет 4 мг 1 раз в сутки. Повышение дозы до 32 мг 1 раз в сутки или до максимально переносимой дозы проводится путем ее удвоения с интервалами не менее 2 нед (см. раздел «Особые указания»).
Особые группы пациентов. Пациентам пожилого возраста и пациентам с нарушением функции почек или печени не требуется изменение начальной дозы препарата.
Применение у детей и подростков. Безопасность и эффективность применения Атаканда® у детей и подростков (в возрасте до 18 лет) не установлены.
Сопутствующая терапия. Атаканд® можно назначать совместно с другими средствами, применяемыми при терапии хронической сердечной недостаточности, например ингибиторами АПФ, бета-адреноблокаторами, диуретиками и сердечными гликозидами (см. разделы «Особые указания», «Фармакодинамика»).
Передозировка
Симптомы: анализ фармакологических свойств препарата позволяет предположить, что основным проявлением передозировки может быть клинически выраженное снижение АД и головокружение. Были описаны отдельные случаи передозировки препарата (до 672 мг кандесартана цилексетила), закончившиеся выздоровлением пациентов без тяжелых последствий.
Лечение: при развитии клинически выраженной артериальной гипотензии необходимо проводить симптоматическое лечение и контролировать состояние пациента. Уложить пациента, приподнять головной конец кровати. При необходимости следует увеличить объем циркулирующей плазмы, например путем в/в введения изотонического раствора хлорида натрия. В случае необходимости могут быть назначены симпатомиметические препараты. Выведение кандесартана с помощью гемодиализа маловероятно.
Особые указания
Нарушение функции почек
На фоне терапии Атакандом®, как и при применении других средств, угнетающих РААС, у некоторых пациентов могут отмечаться нарушения функции почек.
При применении Атаканда® у пациентов с артериальной гипертензией и выраженной почечной недостаточностью рекомендуется периодически контролировать уровень калия и креатинина в сыворотке крови. Клинический опыт применения препарата у пациентов с тяжелым нарушением функции почек или терминальной стадией почечной недостаточности ограничен (Cl креатинина <15 мл/мин).
У пациентов с хронической сердечной недостаточностью необходимо периодически контролировать функцию почек, особенно у пациентов в возрасте 75 лет и старше, а также у пациентов с нарушением функции почек. При повышении дозы Атаканда® также рекомендуется контролировать уровень калия и креатинина.
В клинические исследования Атаканда® при хронической сердечной недостаточности не включались пациенты с уровнем креатинина >265 мкмоль/л (>3 мг/дл).
Совместное применение с ингибиторами АПФ при хронической сердечной недостаточности
При применении кандесартана в комбинации с ингибиторами АПФ может увеличиваться риск развития побочных эффектов, особенно нарушения функции почек и гиперкалиемии (см. раздел «Побочные действия»). В этих случаях необходимо тщательное наблюдение и контроль лабораторных показателей.
Стеноз почечной артерии
У пациентов с двухсторонним стенозом почечной артерии или стенозом артерии единственной почки препараты, оказывающие влияние на РААС, в частности ингибиторы АПФ, могут вызывать повышение уровня мочевины и креатинина в сыворотке крови. Подобные эффекты можно ожидать при назначении антагонистов рецепторов ангиотензина II.
Пересадка почки
Данные о применении Атаканда® у пациентов, недавно перенесших пересадку почки, отсутствуют.
Артериальная гипотензия
У пациентов с хронической сердечной недостаточностью на фоне терапии Атакандом® может развиться артериальная гипотензия. Как и при применении других препаратов, влияющих на РААС, причиной развития артериальной гипотензии у пациентов с артериальной гипертензией может быть уменьшение ОЦК, как наблюдается у пациентов, получающих высокие дозы диуретиков. Поэтому в начале терапии следует соблюдать осторожность и, при необходимости, проводить коррекцию гиповолемии.
Общая анестезия и хирургия
У пациентов, получающих антагонисты ангиотензина II, во время проведения общей анестезии и при хирургических вмешательствах может развиться артериальная гипотензия в результате блокады ренин-ангиотензиновой системы. Очень редко могут отмечаться случаи тяжелой артериальной гипотензии, требующей в/в введения жидкости и/или вазопрессоров.
Стеноз аортального и митрального клапана (обструктивная гипертрофическая кардиомиопатия)
При назначении Атаканда®, как и других вазодилататоров, пациентам с обструктивной гипертрофической кардиомиопатией или гемодинамически значимым стенозом аортального или митрального клапана следует соблюдать осторожность.
Первичный гиперальдостеронизм
Пациенты с первичным гиперальдостеронизмом обычно резистентны к терапии антигипертензивными препаратами, влияющими на РААС. В связи с этим Атаканд® не рекомендуется назначать таким пациентам.
Гиперкалиемия
Клинический опыт применения других препаратов, влияющих на РААС, показывает, что одновременное назначение Атаканда® с калийсберегающими диуретиками, препаратами калия или заменителями соли, содержащими калий, или другими препаратами, которые могут увеличить содержание калия в крови (например гепарин), может привести к развитию гиперкалиемии у пациентов с артериальной гипертензией.
У пациентов с хронической сердечной недостаточностью на фоне терапии Атакандом®, может развиваться гиперкалиемия. При назначении Атаканда® пациентам с хронической сердечной недостаточностью рекомендуется регулярный контроль уровня калия в крови, особенно при совместном назначении с ингибиторами АПФ и калийсберегающими диуретиками.
Общие
Пациенты, у которых сосудистый тонус и функция почек преимущественно зависят от активности РААС (например больные с тяжелой хронической сердечной недостаточностью или заболеваниями почек, включая стеноз почечной артерии), особенно чувствительны к препаратам, действующим на РААС. Назначение подобных средств сопровождается у этих больных резкой артериальной гипотензией, азотемией, олигурией и реже — острой почечной недостаточностью. Возможность развития перечисленных эффектов не может быть исключена и при использовании антагонистов рецепторов ангиотензина II. Резкое снижение АД у больных с ишемической кардиопатией или цереброваскулярными заболеваниями ишемического генеза, при использовании любых антигипертензивных средств, может приводить к развитию инфаркта миокарда или инсульта.
Влияние на способность управлять автомобилем или выполнять работы, требующие повышенной скорости физических и психических реакций. Влияние на способность управлять автомобилем или работать с техникой не изучалось, но фармакодинамические свойства препарата указывают на то, что подобное влияние отсутствует.
При вождении автотранспорта и занятии потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, следует учитывать, что при применении препарата может наблюдаться головокружение и повышенная утомляемость.
Форма выпуска
Таблетки, 8 мг и 16 мг. По 14 табл. в блистере из ПВХ/алюминия; по 2 блистера в картонной пачке.
Производитель
Владелец регистрационного удостоверения: АстраЗенека АБ, SЕ-151 85 Содерталье, Швеция.
Производитель: АстраЗенека АБ, SE-151 85 Содерталье, Швеция.
Выпускающий контроль качества: 1. АстраЗенека АБ, SE-151 85 Содерталье, Швеция; 2. Корден Фарма ГмбХ, Отто-Ханштрассе, D-68723 Планкштадт, Германия; 3. АстраЗенека ГмбХ, Тинсдалер Вег 183, 22880, Ведель, Германия.
Дополнительная информация предоставляется по требованию: представительство компании АстраЗенека ЮК Лимитед, Великобритания, в Москве и ООО АстраЗенека Фармасьютикалз.
125284, Москва, ул. Беговая, 3, стр. 1.
Тел.: (495) 799-56-99; факс: (495) 799-56-98.
Условия отпуска из аптек
По рецепту.
Условия хранения препарата Атаканд®
Хранить в недоступном для детей месте.